¿Por qué hay una tuberculosis tan resistente a los antibióticos?
Gracias a las mutaciones. Así de simple.
Muchos de nosotros asociamos las mutaciones con algo malo o perjudicial para un organismo. Pero las mutaciones son, en realidad, simples cambios de una o más secuencias en el ADN de un determinado individuo. Se dan todo el tiempo, en algunas especies más que en otras. Por ejemplo, se estima que nosotros nacemos con unas 60 nuevas mutaciones respecto a nuestros padres. La mayoría de estos cambios pasan desapercibidos; pero, los que no, pueden llegan a alterar la estructura de unas proteínas llamadas enzimas, las cuales realizan funciones específicas como generar energía, degradar los compuestos tóxicos o producir las materias primas de las células necesarias para vivir.

Las enzimas catalizan reacciones químicas en los seres vivos. Pueden transformar un compuesto Y en uno Z, fusionar dos moléculas (A y B) para formar una sola, pueden degradar moléculas en componentes más sencillos, etc.
Antibióticos contra la TB
Ya hemos hablado bastante sobre la tuberculosis (TB) [aquí y aquí]. Para su tratamiento se requiere de cuatro antibióticos de primera línea:
1. La isoniacida (INH): Inhibe la producción de ácido micólico, un componente esencial de la pared celular de la bacteria. Lo interesante de este antibiótico es que utiliza una enzima propia de la bacteria llamada KatG para poder activarse. Una vez activo, inhibe la acción de la enzima que produce el ácido micólico, llamada InhA.
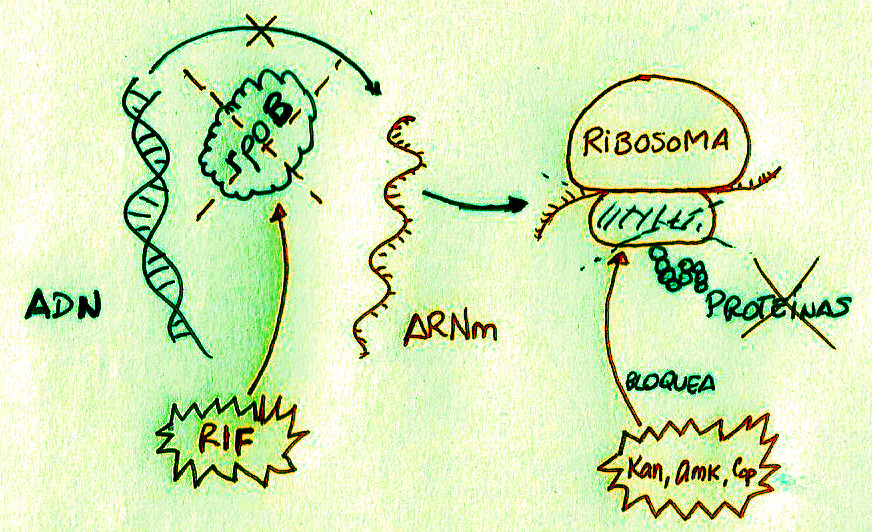
2. La rifampicina (RIF): Inhibe la enzima rpoB que transcribe el ADN en ARN mensajero, un paso esencial para la producción de todas las proteínas bacterianas.
3. El etambutol (EMB): Inhibe a la enzima EmbC que es responsable de transferir el ácido micólico desde el interior de la bacteria a la pared celular para que ésta se forme.
4. La pirazinamida (PZA): Se convierte en ácido pirazinoico dentro de la bacteria —gracias a la acción de la enzima PncA— provocándole una acidez extrema que inhibe su crecimiento.
Todos estos antibióticos se toman de un solo porrazo, de acuerdo a un cronograma específico que puede durar muchos meses sin interrupción. De esta manera se ataca al microbio por todos los frentes, evitando que formen la pared celular que las envuelve y las proteínas necesarias para realizar sus funciones, y provocándoles una acidez que ni con una sal de Andrews® podrían aliviar.
Resistencias
Acabamos de conocer a los antibióticos de primera línea y, como se habrán podido dar cuenta, en todas ellas interviene alguna enzima. Entonces, recordando los primeros párrafos, ¿qué pasaría si estas enzimas mutan? Pues, alterarían su estructura y posiblemente su función.
En algunos casos, la mutación provocaría que la enzima quede inactiva. Esto sería una ventaja para la bacteria si esta mutación se da, por ejemplo, en la enzima PncA porque la pirazinamida perdería su efecto. Esto fue observado varias veces en pacientes con TB de diferentes países (Canadá, Taiwán, Corea del Sur, entre otros).
En otros casos, el cambio de la estructura de la enzima provocaría que el antibiótico no pueda reconocerla y acoplarse a ella para inhibirla, por lo que seguiría cumpliendo con su función sin ningún problema. Si esta mutación se da en la enzima KatG, la bacteria sería resistente a la isoniacida.
Una sola bacteria no puede causar una infección, se necesitan millones de ellas. Cuando están en su fase más activa, cada microbio producirá dos descendientes en unas pocas horas, cada uno con algunas nuevas mutaciones. Es así que en cada generación de bacterias, las probabilidades de que estas mutaciones afecten la estructura de las enzimas que son objetivo de los antibióticos, serán mayores. Sin embargo, es bastante improbable que una sola bacteria adquiera todas las mutaciones necesarias para tolerar dos, tres o cuatro antibióticos a la vez, pero podría ocurrir si es que el paciente no cumple con el tratamiento.
Las mutaciones son la principal fuerza evolutiva y se acumulan a través del tiempo, siendo seleccionadas en función a su utilidad para que una población se adapte a su entorno. Nunca empieza todo desde cero.
Cuando la bacteria adquiere resistencia al menos al la isoniacida y la rifampicina, ya estamos hablando de una tuberculosis multidrogo-resistente (TB-MR).
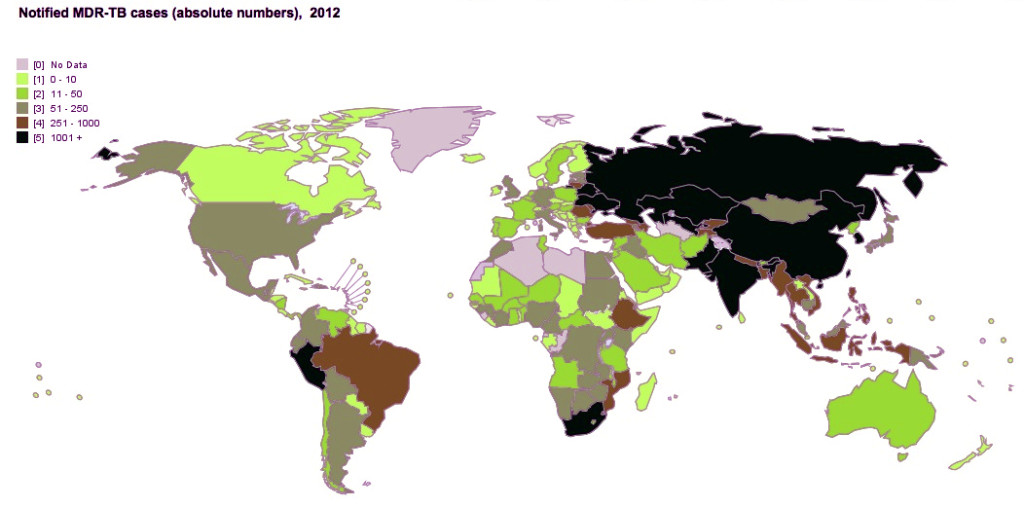
El Perú está entre los países con mayor número de casos de TB-MR en el mundo. Somos el primero en América. Datos de la OMS al 2012. [Click para ampliar]
En este caso se deben usar antibióticos de segunda línea, los cuales son más fuertes, costosos y con peores efectos secundarios. Entre estos antibióticos tenemos:
Los aminoglucósidos (Ej: estreptomicina, amikacina o kanamicina): Inhiben la formación de proteínas de la bacteria porque interfieren con la traducción del ARN mensajero en el ribosoma. También se usa la capreomicina, un antibiótico polipeptídico, que actúa de la misma manera. Estos antibióticos son inyectables.
Las fluoroquinolonas (FLQ), (Ej: moxifloxacina y ciprofloxacina): Inhibe la replicación del ADN, evitando que éste se desenrolle y separe, por lo que la bacteria no puede completar la división celular.
Resistencias extremas
Si creías que la TB-MR era un grave problema para la salud pública, qué pasa cuando esta bacteria además se vuelve resistente a las fluoroquinolonas y al menos a uno de los tres antibióticos inyectables: amikacina, capreomicina o kanamicina. Aquí ya hablamos de una tuberculosis extremadamente resistente (TB-XR). En este caso, los pacientes cuentan con menos opciones para curarse porque los mejores antibióticos para tratar la TB se volvieron inservibles. Además, el tratamiento se vuelve mucho más costoso, pudiendo alcanzar casi medio millón de dólares por paciente, según estimaciones de la CDC.

Gráfico que muestra los antibióticos que se vuelven inefectivos en una TB-XR. Fuente: NIAID-NIH. [Click para ampliar]
El abandono del tratamiento es una de las principales causas por las cuales la tuberculosis se hace cada vez más resistente. Los pocos microbios que de alguna manera lograron sobrevivir a la guerra química incompleta, empiezan a multiplicarse y reemplazar a los microbios susceptibles que cayeron en el campo de batalla. La infección reaparece, pero esta vez con más fuerza. Ya nada los detiene así que lo único que queda es extirparlos de raíz, esto quiere decir, sacar la parte del pulmón afectada por las bacterias. Pero muchas veces esto no es posible puesto que la TB está diseminada por todo el pulmón.
Hace un par de semanas, investigadores del Instituto Nacional de Salud (INS), liderados por el Dr. Heinner Guio, publicaron un interesante estudio en el cual reportan la secuenciación del genoma de una cepa de TB-XR aislada en el país (INS-XDR), que fue comparada con el genoma de otras 16 cepas de TB-XR en el mundo identificando 218 nuevas mutaciones en 125 genes. De todas las mutaciones, unas 14 podrían estar relacionadas con la resistencia a la kanamicina y capreomicina.
Las mutaciones no se dan con el fin de que una especie evolucione o se haga más resistente a los antibióticos, simplemente se dan. Es inherente a la vida misma. Lo que hacen las mutaciones es generar una variabilidad de “formas” sobre las cuales una fuerza selectora actúa.
En este caso, la fuerza selectora son los antibióticos, los cuales están diseñados para matar a todas las bacterias, pero puede darse el caso que unas pocas tengas ciertas mutaciones que las hagan capaces de aguantar un poquito más. Ellas transmitirán esta capacidad a sus descendientes. Si no completamos el tratamiento, ya sea porque nos sentimos mejor o porque lamentablemente no tenemos los recursos para continuar, estas cepas un poco más resistentes proliferarán y adquirirán nuevas mutaciones. Y así, silenciosamente, se volverán invencibles.

:quality(75)/2.blogs.elcomercio.pe/service/img/expresiongenetica/autor.jpg)