¿Hamburguesa in vitro? Todavía no...
Pregunté a una amiga vegetariana si estaría dispuesta a comer una hamburguesa hecha a base de carne desarrollada en el laboratorio. —Yo creo que sí—, me respondió. Y es que muchos vegetarianos evitan comer carne por una cuestión de empatía con los animales. Consideran que la forma cómo son criados (en hacinamiento) y luego sacrificados, les causa sufrimiento.
Por otro lado, cada día más personas toman conciencia del impacto que genera la producción de carne sobre el medio ambiente. Se estima que el 14,5% de las emisiones de gases de efecto invernadero de origen antropogénico se deben a la ganadería. Por ello, los científicos buscan nuevas formas de producir carne de manera mucho más sostenible. Una de ellas es hacerlas en el laboratorio.
Todo empieza con unas cuantas células obtenidas del tejido muscular de un animal (células madre musculares) o de embriones desarrollados por fertilización in vitro (células madre embrionarias), que son colocadas en unos tanques con todos los factores ambientales controlados (temperatura, cantidad de oxígeno, pH, velocidad de agitación, flujo de nutrientes, etc.). Estos tanques son conocidos como biorreactores y aquí las células se encuentran sumergidas en una solución (medio de cultivo) que contiene todos los nutrientes que necesitan para multiplicarse y luego convertirse (diferenciarse) en fibras musculares (miofibras).
A partir de aquí viene lo complicado. Las miofibras generadas deben fusionarse y adquirir la consistencia de la carne. Para ello se les somete a estímulos eléctricos y mecánicos, con el fin de que produzcan las proteínas que caracterizan al tejido muscular.
Requieren además de un sistema vascular (como los vasos capilares) que lleven los nutrientes a todas las células del tejido; así como también, un soporte de un material comestible sobre el cual pueda crecer y adquirir de una forma determinada.
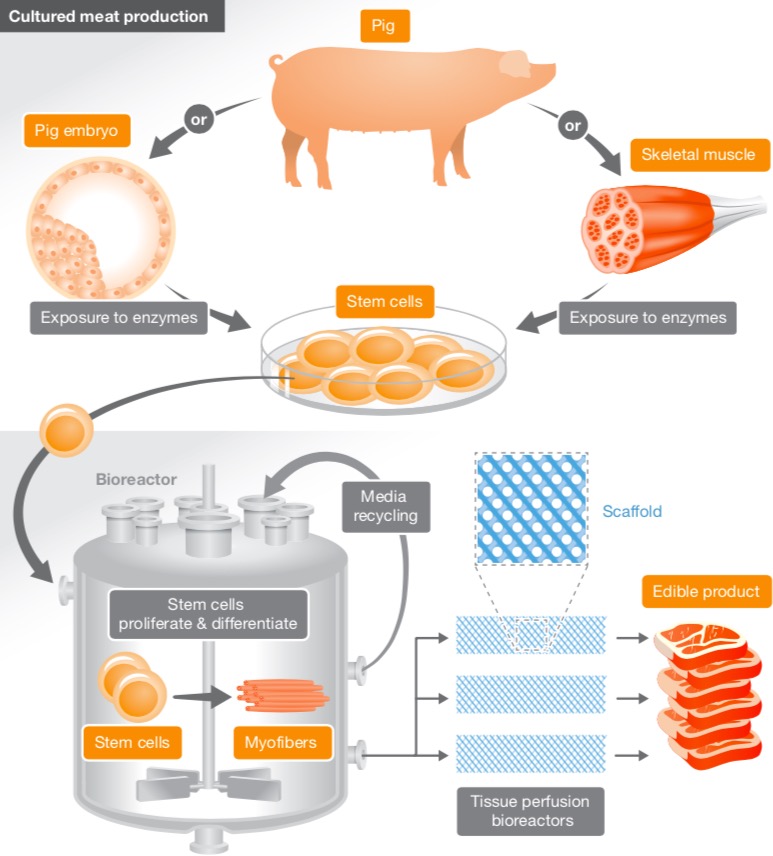
Así se produce la carne en el laboratorio. Fuente: Toumisto, H. (2018).
El problema con la carne in vitro es producirla a gran escala. Los componentes del medio de cultivo son muy costosos, entre ellos, el suero fetal bovino (SFB), el cual se obtiene —irónicamente— del sacrificio de vacas preñadas. Por otro lado, ajustar el diseño y los parámetros de funcionamiento de los biorreactores es muy complicado. No basta con aumentar el tamaño de la olla y añadirle más ingredientes a la sopa.
Si se superan estos inconvenientes, la carne in vitro podría reducir las emisiones de gases de efecto invernadero, el uso de la tierra (para poder destinarlo a la reforestación o la siembra de diversos productos agrícolas) y el consumo de agua (aunque no tanto como la producción de aves de corral). No obstante, en cuanto al consumo de energía, esta sería tan demandante como la carne de res.
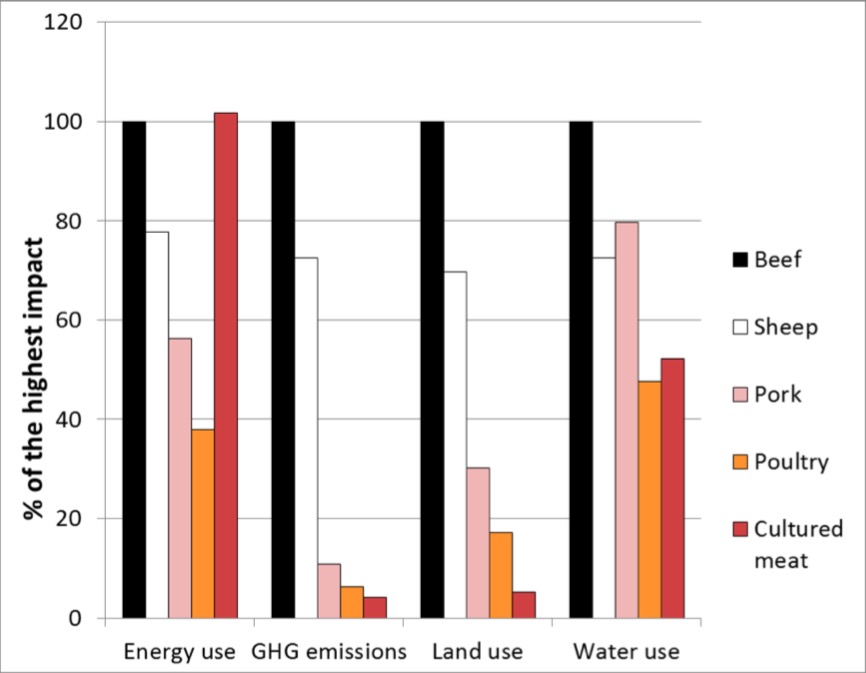
Comparativo del impacto ambiental de las diferentes fuentes de proteína. Fuente: Toumisto et al. (2014).
Otra limitante es que el consumo de carne está asociado fuertemente con factores sociales y culturales complejos, más aún cuando constituyó nuestra principal fuente de nutrientes antes del desarrollo de la agricultura. Además, el sabor y la textura del producto siempre serán características que orientarán la preferencia de los consumidores.
La carne in vitro podría convertirse en una alternativa sostenible a la producción intensiva de carne; aunque todavía queda mucho camino por recorrer. Por otro lado, la producción de carne no necesariamente es mala. En sistemas de producción cerrados resulta beneficioso para el ambiente porque se conservan los pastizales naturales (los cuales capturan el CO2), los desechos orgánicos son usados para fertilizar los suelos agrícolas y producir gas, y los animales son la forma más eficiente de transformar la materia vegetal en nutrientes esenciales fácilmente asimilables para el ser humano.
Referencia:
Toumisto H. 2018. The eco-friendly burguer. EMBO Reports 20: e47395

:quality(75)/2.blogs.elcomercio.pe/service/img/expresiongenetica/autor.jpg)